Exercices de Nomenclature en Chimie Organique avec Corrections Doc
La nomenclature en chimie organique est un ensemble de règles permettant de nommer systématiquement les composés organiques en fonction de leur structure. La norme utilisée à l’international est celle de l’IUPAC (International Union of Pure and Applied Chemistry). Voici un aperçu des règles de base pour les principales familles de composés organiques.
1. Nomenclature des Alcanes
Les alcanes sont des hydrocarbures saturés, c’est-à-dire sans double ou triple liaison. La formule générale est ( C_nH_{2n+2} ). Le nom des alcanes est basé sur le nombre de carbones dans la chaîne principale.
| Nombre de carbones | Nom |
|---|---|
| 1 | Méthane |
| 2 | Éthane |
| 3 | Propane |
| 4 | Butane |
| 5 | Pentane |
| 6 | Hexane |
| 7 | Heptane |
| 8 | Octane |
Exemple :
- ( CH_4 ) : Méthane
- ( CH_3CH_2CH_3 ) : Propane
2. Nomenclature des Alcools
Les alcools contiennent un groupe hydroxyle (-OH). Ils se nomment en ajoutant le suffixe « -ol » au nom de la chaîne principale, et on précise la position de l’hydroxyle si nécessaire.
Exemples :
- ( CH_3OH ) : Méthanol
- ( CH_3CH_2OH ) : Éthanol
- ( CH_3CH(OH)CH_3 ) : Propan-2-ol
3. Nomenclature des Alcènes
Les alcènes sont des hydrocarbures insaturés, contenant une double liaison carbone-carbone. La double liaison est indiquée par le suffixe « -ène », et sa position est spécifiée si la molécule compte plus de trois carbones.
Exemples :
- ( CH_2=CH_2 ) : Éthène
- ( CH_3CH=CH_2 ) : Prop-1-ène
- ( CH_3CH=CHCH_3 ) : But-2-ène
4. Nomenclature des Alcynes
Les alcynes possèdent une triple liaison carbone-carbone et sont nommés avec le suffixe « -yne ». La position de la triple liaison est précisée si nécessaire.
Exemples :
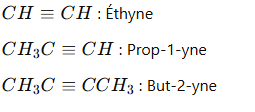
5. Nomenclature des Acides Carboxyliques
Les acides carboxyliques se caractérisent par le groupe carboxyle (-COOH) et se nomment en ajoutant le mot « acide » suivi de la chaîne principale avec le suffixe « -oïque ». Le groupe carboxyle étant toujours en bout de chaîne, il n’est pas nécessaire de préciser sa position.
Exemples :
- ( CH_3COOH ) : Acide éthanoïque (acide acétique)
- ( CH_3CH_2COOH ) : Acide propanoïque
- ( CH_3CH_2CH_2COOH ) : Acide butanoïque
6. Nomenclature des Dérivés Halogénés
Les dérivés halogénés sont des hydrocarbures dans lesquels un ou plusieurs atomes d’hydrogène ont été remplacés par des halogènes (F, Cl, Br, I). Le nom indique la position et le type de l’halogène avec des préfixes comme « fluoro- », « chloro- », « bromo- » ou « iodo- ».
Exemples :
- ( CH_3CH_2CH_2Cl ) : 1-chloropropane
- ( CH_3CH(Br)CH_3 ) : 2-bromopropane
- ( CH_3CH_2CH(I)CH_3 ) : 2-iodobutane
Conseils pour la Nomenclature
- Identifier la chaîne principale : choisir la plus longue chaîne de carbone contenant le groupe fonctionnel prioritaire.
- Numéroter la chaîne : débuter la numérotation du côté le plus proche du groupe fonctionnel le plus prioritaire.
- Nommer les substituants : les alkyles et les halogènes sont nommés et numérotés en ordre alphabétique.
- Utiliser des préfixes multiplicateurs : pour indiquer la présence de plusieurs groupes fonctionnels identiques (di-, tri-, etc.).
La nomenclature en chimie organique nécessite de la pratique pour s’habituer aux règles et exceptions. Ces principes généraux constituent une base essentielle pour nommer les composés organiques de manière précise et cohérente.